See all products
See all products
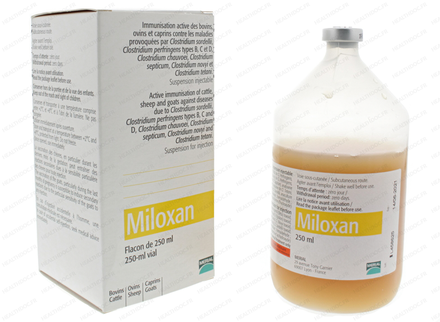
MILOXAN 50 ml
MILOXAN 50 ml
After validating your request, you will have acess to the price of this prescription drug. Learn more To get more information about this vet drug, contact a pharmacist by clicking here.
Product Description
Numbers marketing authorization (No. AMM):
FR/V/6248297 4/1985Code ATCVet:
QI04AB01CIP:
6818233GTIN:
3660000000000Espèces cibles
Indications d'utilisation, en spécifiant les espèces cibles
- Immunisation active contre les maladies provoquées par Clostridium sordellii, Clostridium perfringens types B, C et D, Clostridium chauvoei, Clostridium septicum, Clostridium novyi et Clostridium tetani.
Posologie et voie d'administration
Administrer le vaccin par voie sous-cutanée selon les modalités suivantes :
Ovins : 2 ml
Caprins : 2 ml
Bovins de moins de 4 mois : 2 ml
Bovins de plus de 4 mois : 4 ml
Programme de vaccination :
Primovaccination : 2 injections à 4 semaines d'intervalle.
Rappels : annuel
Chez les animaux gestants : afin de fournir une protection passive des nouveau-nés par l'intermédiaire du colostrum, la seconde injection de primovaccination ou l'injection de rappel doit être administrée durant le dernier tiers de gestation (entre 6 et 2 semaines avant la date présumée de mise-bas).
Chez les jeunes animaux :
- Issus de mères non vaccinées : vaccination à partir de la 2 ème semaine d'âge.
- Issus de mères vaccinées : vaccination à partir de la 8 ème semaine d'âge.
Type of medication
ImmunologicalPharmaceutical form
Injectable suspensionRoute of administration
SubcutaneousPrescription ?
Issuance on prescriptionConditions of drug dispensing
Vaccine : dispensing on prescriptionActive substance
Clostridium novyi Clostridium perfringens Clostridium chauvoei Clostridium septicum Clostridium sordellii Clostridium tetaniContre-indications
Mises en garde particulières à chaque espèce cible
Précautions particulières d'emploi chez l'animal
Précautions particulières à prendre par la personne qui administre le médicament vétérinaire aux animaux
Autres précautions
Effets indésirables (fréquence et gravité)
Utilisation en cas de gravidité, de lactation ou de ponte
Interactions médicamenteuses et autres formes d'interactions
Surdosage (symptômes, conduite d'urgence, antidotes), si nécessaire
Temps d'attente
Incompatibilités
Durée de conservation
Après ouverture : utiliser immédiatement.
Précautions particulières de conservation
Précautions particulières à prendre lors de l'élimination de médicaments vétérinaires non utilisés ou de déchets dérivés de l'utilisation de ces médicaments
Composition qualitative et quantitative
Clostridium perfringens type B (Bêta), anatoxine........................... >= 10,0 UI 1
Clostridium perfringens type D (Epsilon), anatoxine...................... >= 5,0 UI 1
Clostridium septicum , anatoxine.................................................... >= 2,5 UI 1
Clostridium novyi , anatoxine.......................................................... >= 3,5 UI 1
Clostridium tetani , anatoxine.......................................................... >= 2,5 UI 1
Clostridium sordellii , anatoxine...................................................... 90% PC 2
Clostridium chauvoei , anaculture................................................... 90% PC 2
Formaldéhyde................................................................................ <= 3,2 mg
Aluminium...................................................................................... 4,2 mg
(sous forme d'hydroxyde)
Excipient QSP 2 ml
1 UI: titre en anticorps obtenus dans les conditions des monographies de la Ph. Eur.
2 90% PC: 90% de protection à l'épreuve des cobayes vaccinés (selon la monographie de la Ph. Eur. pour Cl. chauvoei ; selon la monographie interne pour Cl. sordellii).
Pour la liste complète des excipients, voir rubrique « Liste des excipients ».
Liste des excipients
Formaldéhyde
Solution de chlorure de sodium
Eau pour préparations injectables
Dénomination du médicament vétérinaire
Composition qualitative et quantitative
Clostridium perfringens type B (Bêta), anatoxine........................... >= 10,0 UI 1
Clostridium perfringens type D (Epsilon), anatoxine...................... >= 5,0 UI 1
Clostridium septicum , anatoxine.................................................... >= 2,5 UI 1
Clostridium novyi , anatoxine.......................................................... >= 3,5 UI 1
Clostridium tetani , anatoxine.......................................................... >= 2,5 UI 1
Clostridium sordellii , anatoxine...................................................... 90% PC 2
Clostridium chauvoei , anaculture................................................... 90% PC 2
Formaldéhyde................................................................................ <= 3,2 mg
Aluminium...................................................................................... 4,2 mg
(sous forme d'hydroxyde)
Excipient QSP 2 ml
1 UI: titre en anticorps obtenus dans les conditions des monographies de la Ph. Eur.
2 90% PC: 90% de protection à l'épreuve des cobayes vaccinés (selon la monographie de la Ph. Eur. pour Cl. chauvoei ; selon la monographie interne pour Cl. sordellii).
Pour la liste complète des excipients, voir rubrique « Liste des excipients ».
Forme pharmaceutique
Espèces cibles
Indications d'utilisation, en spécifiant les espèces cibles
- Immunisation active contre les maladies provoquées par Clostridium sordellii, Clostridium perfringens types B, C et D, Clostridium chauvoei, Clostridium septicum, Clostridium novyi et Clostridium tetani.
Contre-indications
Mises en garde particulières à chaque espèce cible
Précautions particulières d'emploi chez l'animal
Précautions particulières à prendre par la personne qui administre le médicament vétérinaire aux animaux
Autres précautions
Effets indésirables (fréquence et gravité)
Utilisation en cas de gravidité, de lactation ou de ponte
Interactions médicamenteuses et autres formes d'interactions
Posologie et voie d'administration
Administrer le vaccin par voie sous-cutanée selon les modalités suivantes :
Ovins : 2 ml
Caprins : 2 ml
Bovins de moins de 4 mois : 2 ml
Bovins de plus de 4 mois : 4 ml
Programme de vaccination :
Primovaccination : 2 injections à 4 semaines d'intervalle.
Rappels : annuel
Chez les animaux gestants : afin de fournir une protection passive des nouveau-nés par l'intermédiaire du colostrum, la seconde injection de primovaccination ou l'injection de rappel doit être administrée durant le dernier tiers de gestation (entre 6 et 2 semaines avant la date présumée de mise-bas).
Chez les jeunes animaux :
- Issus de mères non vaccinées : vaccination à partir de la 2 ème semaine d'âge.
- Issus de mères vaccinées : vaccination à partir de la 8 ème semaine d'âge.
Surdosage (symptômes, conduite d'urgence, antidotes), si nécessaire
Temps d'attente
Propriétés immunologiques
Vaccin inactivé adjuvé contre les toxi-infections à bactéries anaérobies ( Cl. chauvoei, Cl. novyi, Cl. septicum, Cl. Perfringens type B , Cl. Perfringens typeC , Cl. Perfringens typeD , Cl. sordellii, Cl. tetani ) des ruminants.
Liste des excipients
Formaldéhyde
Solution de chlorure de sodium
Eau pour préparations injectables
Incompatibilités
Durée de conservation
Après ouverture : utiliser immédiatement.
Précautions particulières de conservation
Nature et composition du conditionnement primaire
Flacon verre type II (50 ml)
Flacon polypropylène (100 et 250 ml)
Bouchon dérivé du butyle
Capsule aluminium
Précautions particulières à prendre lors de l'élimination de médicaments vétérinaires non utilisés ou de déchets dérivés de l'utilisation de ces médicaments
Titulaire de l'autorisation de mise sur le marché
29 AVENUE TONY GARNIER
69007 LYON
Numéro(s) d'autorisation de mise sur le marché
Boîte de 1 flacon de 4 ml
Boîte de 10 flacons de 4 ml
Coque de 10 flacons de 4 ml
Boîte de 1 flacon de 50 ml
Boîte de 1 flacon de 100 ml
Boîte de 1 flacon de 250 ml
Toutes les présentations peuvent ne pas être commercialisées.
Date de première autorisation/renouvellement de l'autorisation
Date de mise à jour du texte
 See all products
See all products
Merial est une société de santé animale, fabrique et commercialise des produits de santé, des produits pharmaceutiques et des vaccins pour animaux. Merial LLC recherche, développe, fabrique et distribue des produits pharmaceutiques et biologiques pour la santé animale et des animaux de compagnie.
"Des médicaments pharmaceutiques et des vaccins biologiques aux produits de bien-être, nous développons des solutions intelligentes pour un large éventail d'espèces et de problèmes de santé animale.Nous avons été pionniers en matière de changement de jeu en médecine vétérinaire - et nous recherchons les besoins de nos clients. l'avenir." merial.com
See more information
Espèces cibles
Indications d'utilisation, en spécifiant les espèces cibles
- Immunisation active contre les maladies provoquées par Clostridium sordellii, Clostridium perfringens types B, C et D, Clostridium chauvoei, Clostridium septicum, Clostridium novyi et Clostridium tetani.
Posologie et voie d'administration
Administrer le vaccin par voie sous-cutanée selon les modalités suivantes :
Ovins : 2 ml
Caprins : 2 ml
Bovins de moins de 4 mois : 2 ml
Bovins de plus de 4 mois : 4 ml
Programme de vaccination :
Primovaccination : 2 injections à 4 semaines d'intervalle.
Rappels : annuel
Chez les animaux gestants : afin de fournir une protection passive des nouveau-nés par l'intermédiaire du colostrum, la seconde injection de primovaccination ou l'injection de rappel doit être administrée durant le dernier tiers de gestation (entre 6 et 2 semaines avant la date présumée de mise-bas).
Chez les jeunes animaux :
- Issus de mères non vaccinées : vaccination à partir de la 2 ème semaine d'âge.
- Issus de mères vaccinées : vaccination à partir de la 8 ème semaine d'âge.
-
Species
Goats Cattle Sheep -
For Who ?
Cattle Caprine Sheep (male) -
Type of medication
Immunological -
Pharmaceutical form
Injectable suspension -
Route of administration
Subcutaneous -
Prescription ?
Issuance on prescription -
Conditions of drug dispensing
Vaccine : dispensing on prescription -
Active substance
Clostridium novyi Clostridium perfringens Clostridium chauvoei Clostridium septicum Clostridium sordellii Clostridium tetani -
Category
Veterinary drugs Immunity, Vaccines, Sera
Contre-indications
Mises en garde particulières à chaque espèce cible
Précautions particulières d'emploi chez l'animal
Précautions particulières à prendre par la personne qui administre le médicament vétérinaire aux animaux
Autres précautions
Effets indésirables (fréquence et gravité)
Utilisation en cas de gravidité, de lactation ou de ponte
Interactions médicamenteuses et autres formes d'interactions
Surdosage (symptômes, conduite d'urgence, antidotes), si nécessaire
Temps d'attente
Incompatibilités
Durée de conservation
Après ouverture : utiliser immédiatement.
Précautions particulières de conservation
Précautions particulières à prendre lors de l'élimination de médicaments vétérinaires non utilisés ou de déchets dérivés de l'utilisation de ces médicaments
Composition qualitative et quantitative
Clostridium perfringens type B (Bêta), anatoxine........................... >= 10,0 UI 1
Clostridium perfringens type D (Epsilon), anatoxine...................... >= 5,0 UI 1
Clostridium septicum , anatoxine.................................................... >= 2,5 UI 1
Clostridium novyi , anatoxine.......................................................... >= 3,5 UI 1
Clostridium tetani , anatoxine.......................................................... >= 2,5 UI 1
Clostridium sordellii , anatoxine...................................................... 90% PC 2
Clostridium chauvoei , anaculture................................................... 90% PC 2
Formaldéhyde................................................................................ <= 3,2 mg
Aluminium...................................................................................... 4,2 mg
(sous forme d'hydroxyde)
Excipient QSP 2 ml
1 UI: titre en anticorps obtenus dans les conditions des monographies de la Ph. Eur.
2 90% PC: 90% de protection à l'épreuve des cobayes vaccinés (selon la monographie de la Ph. Eur. pour Cl. chauvoei ; selon la monographie interne pour Cl. sordellii).
Pour la liste complète des excipients, voir rubrique « Liste des excipients ».
Liste des excipients
Formaldéhyde
Solution de chlorure de sodium
Eau pour préparations injectables
Dénomination du médicament vétérinaire
Composition qualitative et quantitative
Clostridium perfringens type B (Bêta), anatoxine........................... >= 10,0 UI 1
Clostridium perfringens type D (Epsilon), anatoxine...................... >= 5,0 UI 1
Clostridium septicum , anatoxine.................................................... >= 2,5 UI 1
Clostridium novyi , anatoxine.......................................................... >= 3,5 UI 1
Clostridium tetani , anatoxine.......................................................... >= 2,5 UI 1
Clostridium sordellii , anatoxine...................................................... 90% PC 2
Clostridium chauvoei , anaculture................................................... 90% PC 2
Formaldéhyde................................................................................ <= 3,2 mg
Aluminium...................................................................................... 4,2 mg
(sous forme d'hydroxyde)
Excipient QSP 2 ml
1 UI: titre en anticorps obtenus dans les conditions des monographies de la Ph. Eur.
2 90% PC: 90% de protection à l'épreuve des cobayes vaccinés (selon la monographie de la Ph. Eur. pour Cl. chauvoei ; selon la monographie interne pour Cl. sordellii).
Pour la liste complète des excipients, voir rubrique « Liste des excipients ».
Forme pharmaceutique
Espèces cibles
Indications d'utilisation, en spécifiant les espèces cibles
- Immunisation active contre les maladies provoquées par Clostridium sordellii, Clostridium perfringens types B, C et D, Clostridium chauvoei, Clostridium septicum, Clostridium novyi et Clostridium tetani.
Contre-indications
Mises en garde particulières à chaque espèce cible
Précautions particulières d'emploi chez l'animal
Précautions particulières à prendre par la personne qui administre le médicament vétérinaire aux animaux
Autres précautions
Effets indésirables (fréquence et gravité)
Utilisation en cas de gravidité, de lactation ou de ponte
Interactions médicamenteuses et autres formes d'interactions
Posologie et voie d'administration
Administrer le vaccin par voie sous-cutanée selon les modalités suivantes :
Ovins : 2 ml
Caprins : 2 ml
Bovins de moins de 4 mois : 2 ml
Bovins de plus de 4 mois : 4 ml
Programme de vaccination :
Primovaccination : 2 injections à 4 semaines d'intervalle.
Rappels : annuel
Chez les animaux gestants : afin de fournir une protection passive des nouveau-nés par l'intermédiaire du colostrum, la seconde injection de primovaccination ou l'injection de rappel doit être administrée durant le dernier tiers de gestation (entre 6 et 2 semaines avant la date présumée de mise-bas).
Chez les jeunes animaux :
- Issus de mères non vaccinées : vaccination à partir de la 2 ème semaine d'âge.
- Issus de mères vaccinées : vaccination à partir de la 8 ème semaine d'âge.
Surdosage (symptômes, conduite d'urgence, antidotes), si nécessaire
Temps d'attente
Propriétés immunologiques
Vaccin inactivé adjuvé contre les toxi-infections à bactéries anaérobies ( Cl. chauvoei, Cl. novyi, Cl. septicum, Cl. Perfringens type B , Cl. Perfringens typeC , Cl. Perfringens typeD , Cl. sordellii, Cl. tetani ) des ruminants.
Liste des excipients
Formaldéhyde
Solution de chlorure de sodium
Eau pour préparations injectables
Incompatibilités
Durée de conservation
Après ouverture : utiliser immédiatement.
Précautions particulières de conservation
Nature et composition du conditionnement primaire
Flacon verre type II (50 ml)
Flacon polypropylène (100 et 250 ml)
Bouchon dérivé du butyle
Capsule aluminium
Précautions particulières à prendre lors de l'élimination de médicaments vétérinaires non utilisés ou de déchets dérivés de l'utilisation de ces médicaments
Titulaire de l'autorisation de mise sur le marché
29 AVENUE TONY GARNIER
69007 LYON
Numéro(s) d'autorisation de mise sur le marché
Boîte de 1 flacon de 4 ml
Boîte de 10 flacons de 4 ml
Coque de 10 flacons de 4 ml
Boîte de 1 flacon de 50 ml
Boîte de 1 flacon de 100 ml
Boîte de 1 flacon de 250 ml
Toutes les présentations peuvent ne pas être commercialisées.
Date de première autorisation/renouvellement de l'autorisation
Date de mise à jour du texte
 See all products
See all products
Merial est une société de santé animale, fabrique et commercialise des produits de santé, des produits pharmaceutiques et des vaccins pour animaux. Merial LLC recherche, développe, fabrique et distribue des produits pharmaceutiques et biologiques pour la santé animale et des animaux de compagnie.
"Des médicaments pharmaceutiques et des vaccins biologiques aux produits de bien-être, nous développons des solutions intelligentes pour un large éventail d'espèces et de problèmes de santé animale.Nous avons été pionniers en matière de changement de jeu en médecine vétérinaire - et nous recherchons les besoins de nos clients. l'avenir." merial.com
See more information
More about this product
More about this product
This product does not have any reviews yet
Questions (0)
Ask a questionThis product does not have any Questions and Answers yet
Reviews 0
Questions 0